本期看點(diǎn)
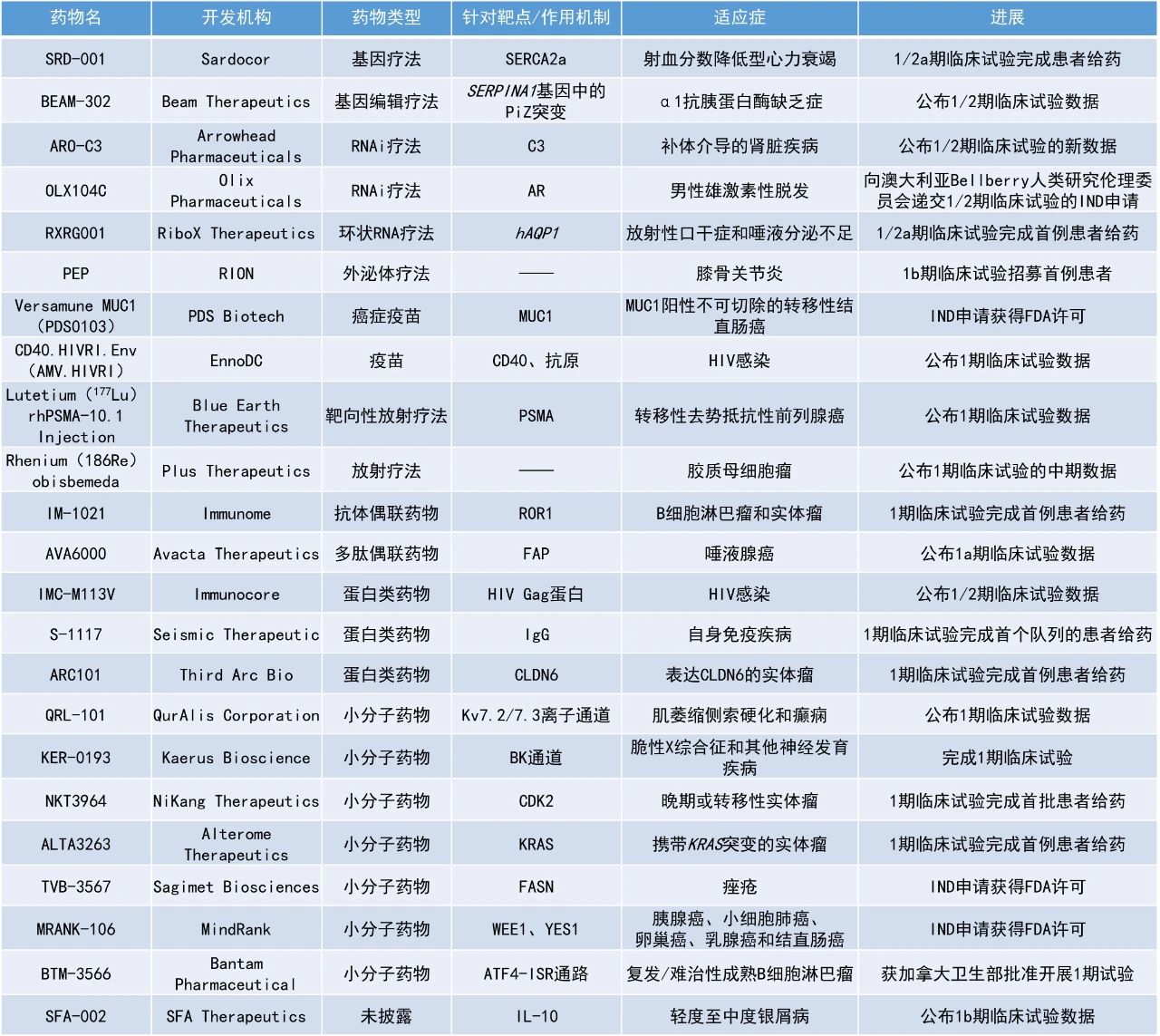
AVA6000:公布1a期臨床試驗(yàn)數(shù)據(jù)
Avacta Therapeutics公司宣布,其在研多肽偶聯(lián)藥物AVA6000在治療唾液腺癌患者的1a期臨床試驗(yàn)中獲得積極數(shù)據(jù),該公司已開(kāi)始招募1b期擴(kuò)展隊(duì)列,多名患者接受了治療。唾液腺癌是一種在轉(zhuǎn)移性階段尚無(wú)標(biāo)準(zhǔn)治療方案的疾病。AVA6000是Avacta研發(fā)管線(xiàn)中的首個(gè)多肽偶聯(lián)藥物,由阿霉素(doxorubicin)與Avacta專(zhuān)有的pre|CISION多肽偶聯(lián)而成,該多肽可在腫瘤微環(huán)境中由成纖維細(xì)胞激活蛋白-α(FAP)特異性切割。FAP在大多數(shù)實(shí)體瘤中,與健康組織相比表達(dá)水平顯著升高。Avacta的多肽偶聯(lián)藥物利用這一特征在腫瘤微環(huán)境中特異性釋放活性藥物,從而降低系統(tǒng)暴露和毒性,為患者提供最佳治療效果。
此次公布的數(shù)據(jù)顯示,與常規(guī)治療患者相比,在接受AVA6000治療的唾液腺癌患者中觀(guān)察到令人鼓舞的PFS數(shù)據(jù)。在接受250 mg/m²及以上劑量治療的11名唾液腺癌患者中,DCR達(dá)91%,5名患者腫瘤顯著縮小,其中包括1例部分緩解(PR,腫瘤縮小超過(guò)30%)和4例輕微緩解(MR,腫瘤縮小10%-29%)。中位隨訪(fǎng)時(shí)間約為5個(gè)月,尚未達(dá)到中位PFS,而先前研究中使用常規(guī)抗癌治療患者的中位PFS約為3.5個(gè)月。安全性方面,AVA6000的耐受性良好,沒(méi)有觀(guān)察到與常規(guī)劑量阿霉素相關(guān)的嚴(yán)重心臟毒性事件。
Rhenium(186Re)obisbemeda:公布1期臨床試驗(yàn)的中期數(shù)據(jù)
Plus Therapeutics公司宣布,其主打放射治療藥物Rhenium(186Re)obisbemeda治療膠質(zhì)母細(xì)胞瘤的1期臨床試驗(yàn)結(jié)果已發(fā)表在Nature Communications上。該療法是一款新型可注射放療藥物,專(zhuān)門(mén)配制用于以安全、有效和方便的方式在中樞神經(jīng)系統(tǒng)(CNS)腫瘤中遞送專(zhuān)一靶向的高劑量輻射,以?xún)?yōu)化患者臨床結(jié)局。由于186Re的半衰期短,具有破壞癌組織的β放射能和可用于活體成像的γ放射能,是CNS治療應(yīng)用的理想放射性同位素。
此次公布的結(jié)果顯示,21名患者的中位OS為11個(gè)月,12名接受超過(guò)100 Gy輻射劑量的患者的中位OS為17個(gè)月,是接受標(biāo)準(zhǔn)治療的復(fù)發(fā)性GBM患者的中位OS(約8個(gè)月)的兩倍多。安全性方面,未觀(guān)察到劑量限制性毒性,且大多數(shù)不良事件與研究治療無(wú)關(guān)。
BEAM-302:公布1/2期臨床試驗(yàn)數(shù)據(jù)
Beam Therapeutics公布了在研單堿基編輯療法BEAM-302用于治療α1抗胰蛋白酶缺乏癥(AATD)患者的1/2期臨床試驗(yàn)結(jié)果。BEAM-302是一種針對(duì)肝臟的脂質(zhì)納米顆粒(LNP)配方,內(nèi)含指導(dǎo)RNA(gRNA)和編碼堿基編輯器的mRNA,旨在修正致病的PiZ突變。新聞稿指出,這是首個(gè)利用堿基編輯療法,在體內(nèi)糾正致病基因突變的臨床試驗(yàn)結(jié)果,代表著體內(nèi)堿基編輯療法的臨床概念驗(yàn)證。
此次公布的結(jié)果顯示,在單次輸注BEAM-302后,觀(guān)察到血液循環(huán)中總α-1抗胰蛋白酶(AAT)迅速、持久且呈劑量依賴(lài)性增加,新產(chǎn)生的具有治療水平的修正蛋白AAT,以及突變型AAT的減少。在接受治療后第7天便觀(guān)察到總AAT的變化,第21天左右達(dá)到平臺(tái)期,并在隨訪(fǎng)期間持續(xù)存在。中性粒細(xì)胞彈性蛋白酶抑制及結(jié)合檢測(cè)均證實(shí),增加的AAT具有功能性。在迄今探索的所有劑量水平下,BEAM-302治療均顯示出良好的耐受性和可接受的安全性。
IMC-M113V:公布1/2期臨床試驗(yàn)數(shù)據(jù)
Immunocore公司公布了其在研療法IMC-M113V治療HIV感染者的1/2期臨床試驗(yàn)的初步數(shù)據(jù)。IMC-M113V利用一種T細(xì)胞受體與HIV感染免疫細(xì)胞上的HLA-A*02:01-Gag復(fù)合物結(jié)合。該分子的抗CD3效應(yīng)臂隨后招募T細(xì)胞摧毀含有整合HIV DNA的CD4陽(yáng)性細(xì)胞,消滅所謂的病毒儲(chǔ)存庫(kù)。
數(shù)據(jù)顯示,IMC-M113V耐受性良好,并在中斷抗逆轉(zhuǎn)錄病毒治療(ART)后呈現(xiàn)劑量依賴(lài)性控制病毒的跡象。在15名可評(píng)估的HIV感染者中,120微克隊(duì)列中1人、300微克隊(duì)列中2人在分析性ART治療中斷(ATI)期間觀(guān)察到延遲病毒反彈的情況。這3名顯示病毒控制的患者在第8周的病毒載量約為200 c/mL。此外,這3名患者中有2人在預(yù)先規(guī)定的12周ATI期間始終未接受ART治療。該試驗(yàn)的多次遞增劑量(MAD)部分仍在進(jìn)行中,正在評(píng)估更高劑量,隨后還將設(shè)立一個(gè)或多個(gè)劑量的擴(kuò)展隊(duì)列。
QRL-101:公布1期臨床試驗(yàn)數(shù)據(jù)
QurAlis Corporation公司宣布,其QRL-101的1期機(jī)制驗(yàn)證(PoM)臨床試驗(yàn)在健康受試者中取得了積極的頂線(xiàn)數(shù)據(jù),該試驗(yàn)旨在評(píng)估與肌萎縮側(cè)索硬化(ALS)和癲癇相關(guān)的生物標(biāo)志物。QRL-101是一種潛在“best-in-class”的選擇性Kv7.2/7.3離子通道開(kāi)放劑,用于治療ALS患者由于過(guò)度興奮引起的疾病進(jìn)展,這種現(xiàn)象在散發(fā)性和遺傳性ALS中均有發(fā)生,多數(shù)由KCNQ2基因mRNA前體的錯(cuò)誤剪接引起。Kv7通道也是經(jīng)臨床驗(yàn)證的調(diào)節(jié)癲癇過(guò)度興奮狀態(tài)的有效靶點(diǎn)。體內(nèi)和體外研究表明,與選擇性較差的第一代Kv7.2/7.3通道開(kāi)放劑ezogabine相比,QRL-101顯示出更高的效力,并可能引發(fā)更少的臨床不良事件。
此次公布的結(jié)果顯示,QRL-101在ALS相關(guān)的主要終點(diǎn)——運(yùn)動(dòng)神經(jīng)興奮性閾值追蹤(mNETT)強(qiáng)度-時(shí)間常數(shù)(SDTC)上表現(xiàn)出劑量依賴(lài)性的顯著降低,降幅比第一代Kv7.2/7.3通道開(kāi)放劑在ALS患者中的單劑量研究結(jié)果高出約50%。此外,QRL-101對(duì)癲癇相關(guān)的多個(gè)次要和探索性終點(diǎn)也顯示出顯著影響,表明其能有效透過(guò)血腦屏障并具有潛在的抗癲癇作用。安全性方面,QRL-101的安全性和耐受性與其之前的研究結(jié)果一致,未報(bào)告嚴(yán)重不良事件或因不良事件導(dǎo)致的停藥。
RXRG001:1/2a期臨床試驗(yàn)完成首例患者給藥
轉(zhuǎn)錄本生物科技有限公司(RiboX Therapeutics,簡(jiǎn)稱(chēng)RiboX)宣布,RXRG001用于治療輻射誘導(dǎo)的口干癥和唾液分泌不足的1/2a期臨床試驗(yàn)已完成首例患者給藥。RXRG001是RiboX自主研發(fā)的由LNP包裹的環(huán)形RNA藥物,通過(guò)LNP遞送環(huán)形RNA在唾液腺中表達(dá)水通道蛋白AQP1增強(qiáng)透水性,從而提高進(jìn)入口腔中的唾液流量及流速,改善患者口干癥狀。臨床前研究顯示,RXRG001展現(xiàn)了持久療效同時(shí)具備良好的耐受性和安全性。單次給藥后可顯著增加唾液流量,并且效果可持續(xù)長(zhǎng)達(dá)四周。新聞稿指出,RXRG001是全球首個(gè)獲FDA許可進(jìn)入臨床試驗(yàn)的環(huán)形RNA療法。
TVB-3567:IND申請(qǐng)獲得FDA許可
Sagimet Biosciences公司宣布,其用于治療痤瘡的脂肪酸合成酶(FASN)抑制劑TVB-3567的IND申請(qǐng)已獲得批準(zhǔn)。TVB-3567是一種強(qiáng)效的選擇性小分子FASN抑制劑,計(jì)劃于2025年開(kāi)始首次人體1期臨床試驗(yàn)。痤瘡的發(fā)生與皮膚中皮脂分泌增加密切相關(guān)。FASN是從頭脂肪生成途徑中的最后一步,該途徑產(chǎn)生約80%的皮脂脂質(zhì)。先前的臨床前和臨床研究表明,F(xiàn)ASN抑制劑可以改善皮脂成分并顯著減少痤瘡病變,有潛力作為治療痤瘡的靶點(diǎn)。
四川省醫(yī)藥保化品質(zhì)量管理協(xié)會(huì)組織召開(kāi)
2025版《中國(guó)藥典》將于2025年10月..關(guān)于舉辦四川省藥品生產(chǎn)企業(yè)擬新任質(zhì)量
各相關(guān)企業(yè): 新修訂的《中華人..四川省醫(yī)藥保化品質(zhì)量管理協(xié)會(huì)召開(kāi)第七
四川省醫(yī)藥保化品質(zhì)量管理協(xié)會(huì)第七..“兩新聯(lián)萬(wàn)家,黨建助振興”甘孜行活動(dòng)
為深入貫徹落實(shí)省委兩新工委、省市..學(xué)習(xí)傳達(dá)中央八項(xiàng)規(guī)定精神專(zhuān)題會(huì)議
2025年4月22日,協(xié)會(huì)黨支部組織召..關(guān)于收取2025年度會(huì)費(fèi)的通知
各會(huì)員單位: 在過(guò)去的一年里,..四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)急指
四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)..四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)急指
四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)..