疾病控制率達90%的創新療法;靶點作用率達95%的PI3Kα共價抑制劑…… | 一周盤點
發布時間: 2025-01-21 來源: 藥明康德
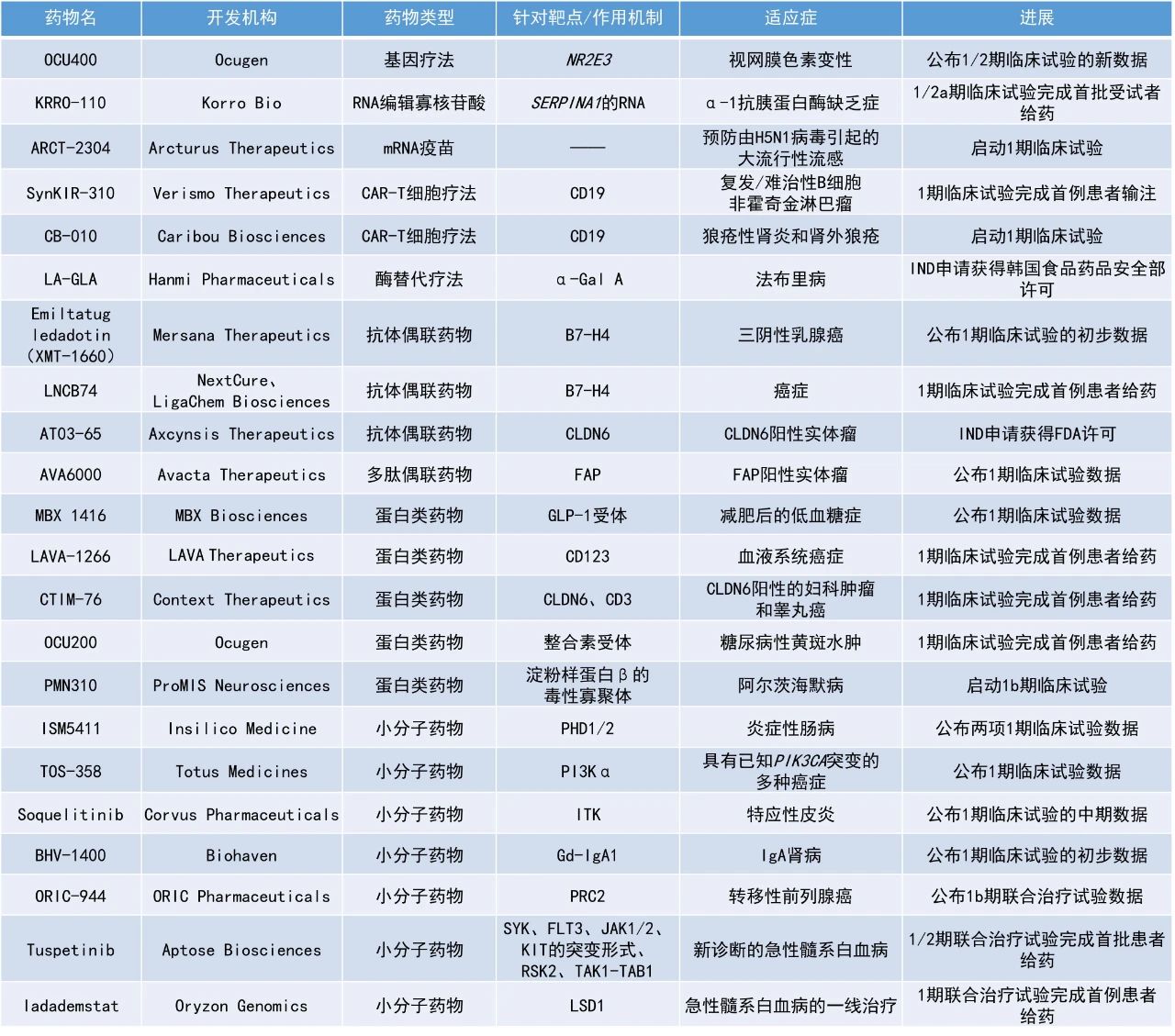
1. 多肽偶聯藥物(PDC)AVA6000在治療唾液腺癌(SGC)患者的1a期臨床試驗中獲得積極數據,疾病控制率(DCR)達90%。2. 蛋白降解藥物BHV-1400在首個人體臨床試驗中獲得積極結果,在最低劑量下只需一次注射,就可在4小時內將致病抗體水平降低60%。3. PI3Kα共價抑制劑TOS-358在一項1期臨床試驗中對PI3Kα的靶點作用率達到95%。
Avacta Therapeutics公司宣布,其在研多肽偶聯藥物AVA6000在治療唾液腺癌患者的1a期臨床試驗中獲得積極數據。唾液腺癌是一種在轉移性階段尚無標準治療方案的疾病。AVA6000是Avacta研發管線中的首個多肽偶聯藥物,由阿霉素(doxorubicin)與Avacta專有的pre|CISION多肽偶聯而成,該多肽可在腫瘤微環境中由成纖維細胞激活蛋白-α(FAP)特異性切割。FAP在大多數實體瘤中,與健康組織相比表達水平顯著升高。Avacta的多肽偶聯藥物利用這一特征在腫瘤微環境中特異性釋放活性藥物,從而降低系統暴露和毒性,為患者提供最佳治療效果。此次公布的數據顯示,AVA6000在唾液腺癌患者中實現了顯著且具有臨床意義的腫瘤縮小。在接受250 mg/m²及以上劑量治療的10名唾液腺癌患者中,DCR達90%,5名患者腫瘤顯著縮小,其中包括一例部分緩解(PR,腫瘤縮小45%)和四例輕微緩解(MR,腫瘤縮小10%-19.5%)。安全性方面,在每兩周一次和每三周一次兩個劑量組中,AVA6000的耐受性良好,與常規劑量阿霉素相比,其血液學和心臟毒性明顯降低。目前尚未在任一劑量組中確定最大耐受劑量(MTD)。Biohaven公司公布了其蛋白降解藥物管線中的雙特異性分子BHV-1400的最新結果。BHV-1400是一款基于耶魯大學(Yale University)的MoDE技術的雙特異性分子,它的一端與半乳糖缺乏型IgA1(Gd-IgA1)抗體結合,另一端與肝細胞表面的去唾液酸糖蛋白受體(ASGPR)結合。ASGPR介導肝細胞通過內吞過程,將靶點蛋白吞入細胞內進行降解。IgA腎病是由于Gd-IgA1的過度生產造成的,BHV-1400通過降低血液循環和腎臟中的Gd-IgA1水平,有望從根源治療IgA腎病。此次公布的初步數據顯示,BHV-1400在首個人體臨床試驗中獲得積極結果,在最低劑量下只需一次注射,就可在4小時內將致病抗體水平降低60%。在某些患者中,觀察到在8小時內將Gd-IgA1水平降低70%。此外,Gd-IgA1水平的降低在單次注射后可維持數天。安全性方面,迄今為止,BHV-1400在1期臨床試驗中的安全性和耐受性良好,未發現具有臨床意義的先天和適應性免疫力的變化,并且未觀察到劑量限制性毒性。這項研究將繼續提高BHV-1400的劑量,探索降低Gd-IgA1水平的范圍。基于該研究的積極結果,該公司還計劃直接啟動關鍵性臨床試驗,評估BHV-1400治療IgA腎病的療效和安全性。Totus Medicines公司公布了其在研PI3Kα共價抑制劑TOS-358的1期臨床試驗數據。TOS-358是一款具高度特異性、強效的PI3Kα抑制劑,可在臨床前模型中實現近100%的PI3Kα抑制,誘導帶有PI3Kα突變的異種移植實體瘤的細胞死亡,包含結直腸癌、肺癌、乳腺癌、卵巢癌、食管癌、頭頸癌,且幾乎沒有觀察到非靶向抑制。此次公布的研究結果表明,TOS-358在低至5 mg每日兩次(BID)的劑量下具有泛突變臨床活性,對PI3Kα的靶點作用率達到95%,且觀察到未經確認的完全緩解(CR)。安全性方面,未報道3/4級毒性。值得注意的是,幾名接受給藥的患者現在已超過6個月未發生進展。在成功完成1期劑量遞增研究后,該公司現在啟動了一項擴展研究,針對乳腺癌、子宮內膜癌、尿路上皮癌和頭頸癌。ORIC Pharmaceuticals公司公布了其選擇性PRC2別構抑制劑ORIC-944聯用阿帕魯胺治療轉移性去勢抵抗性前列腺癌(mCRPC)的1b期臨床試驗數據。截至2024年12月10日的數據,6例患者中有3例達到確認的PSA50應答(即PSA水平降低50%),其中2例達到確認的PSA90應答。所有PSA應答均維持≥12周,其中包括一例在38周時仍然持續的、確認的PSA90應答。Soquelitinib:公布1期臨床試驗的中期數據Corvus Pharmaceuticals公司公布了其小分子白細胞介素-2誘導的T細胞激酶(ITK)抑制劑soquelitinib用于治療中度至重度特應性皮炎的1期臨床試驗的新中期數據。ITK是一種主要表達于T細胞中的酶,在T細胞和自然殺傷(NK)細胞的免疫功能中起重要作用。通過抑制ITK,soquelitinib有望抑制自身免疫和炎癥反應。此次公布的結果顯示,與安慰劑相比,soquelitinib治療組在研究者總體評估(IGA)評分為0/1(皮膚癥狀清除或幾乎清除)和濕疹面積和嚴重度指數較基線減少75%(EASI 75)這些臨床終點方面顯示出良好的療效特征。在soquelitinib組的19例患者中,26%的患者達到IGA 0/1,37%的患者達到EASI 75。在安慰劑組的7例患者中,沒有人達到IGA 0/1,也沒有人達到EASI 75。安全性方面,未觀察到明顯的安全問題,也未發現臨床上顯著的實驗室檢測異常。英矽智能(Insilico Medicine)公司宣布,其自主研發的候選藥物ISM5411已完成在澳大利亞和中國開展的兩項1期研究,并取得了積極的初步結果。ISM5411是一種潛在用于治療炎癥性腸病(IBD)的小分子抑制劑,靶向PHD1/2靶點且具有新穎的分子結構,該候選藥物設計和優化得到了英矽智能生成化學平臺Chemistry42的支持。此次公布的結果顯示,在所有劑量組中ISM5411均表現出良好的安全性和耐受性,并初步驗證了腸道限制性藥代動力學(PK)特征。基于1期臨床試驗的積極結果,英矽智能預計將于2025年下半年啟動一項評估ISM5411在活動性潰瘍性結腸炎患者中的2期臨床試驗。MBX Biosciences公司公布了在健康成年受試者中開展的MBX 1416單劑量遞增和多劑量遞增臨床試驗的積極結果。MBX 1416是一種長效胰高血糖素樣肽1(GLP-1)受體拮抗劑,用于治療減肥后的低血糖癥(PBH)。MBX 1416采用MBX公司新穎、專有的精準內分泌肽(PEP)平臺設計,旨在防止PBH患者發生嚴重低血糖,使他們能夠過上更健康、更獨立的生活。此次公布的結果顯示,MBX 1416通常安全性和耐受性良好,并且具有良好的藥代動力學特征,支持每周一次給藥。基于這些結果,該公司計劃于2025年下半年在PBH患者中啟動一項2期研究,以進一步優化劑量。
