12月25日,中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心(CDE)官網(wǎng)公示,勃林格殷格翰(Boehringer Ingelheim)申報(bào)的宗格替尼片(BI 1810631片)擬納入優(yōu)先審評(píng),擬定適應(yīng)癥為治療攜帶HER2(ERBB2)激活突變且既往接受過(guò)系統(tǒng)治療的不可切除或轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)成人患者。
公開資料顯示,宗格替尼(zongertinib)是一種口服選擇性HER2酪氨酸激酶抑制劑(TKI)。中國(guó)生物制藥于今年4月通過(guò)合作與勃林格殷格翰共同在中國(guó)大陸地區(qū)研發(fā)和商業(yè)化多款腫瘤藥物管線,包括這款宗格替尼。
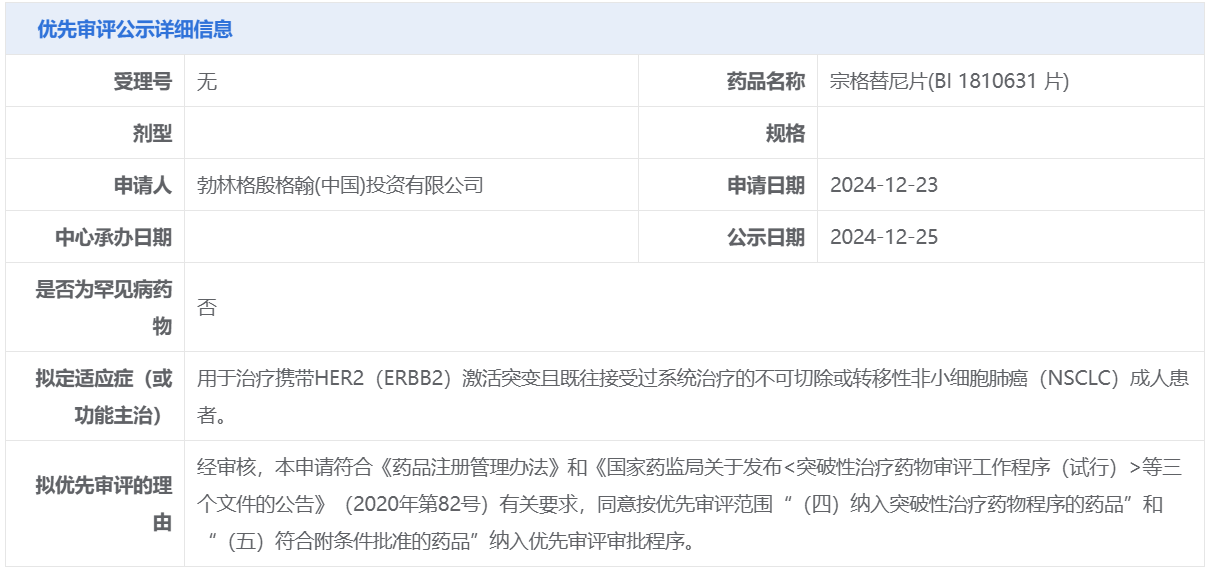 截圖來(lái)源:CDE官網(wǎng)
截圖來(lái)源:CDE官網(wǎng)
HER2突變存在于2%~4%的NSCLC腫瘤中,約50%發(fā)生在酪氨酸激酶結(jié)構(gòu)域(TKD)中。公開資料顯示,HER2突變陽(yáng)性NSCLC患者的一線標(biāo)準(zhǔn)治療為鉑類化療±免疫治療,患者缺少相應(yīng)的靶向療法。
宗格替尼是一種選擇性HER2特異性抑制劑,能與野生型和突變型HER2受體(包括20號(hào)外顯子突變)的酪氨酸激酶結(jié)構(gòu)域共價(jià)結(jié)合,同時(shí)不影響野生型表皮生長(zhǎng)因子受體(EGFR)。HER2 TKI選擇性的提高可能會(huì)帶來(lái)更好的耐受性和療效。目前,美國(guó)FDA已授予該產(chǎn)品快速通道資格,用于治療HER2突變且在鉑類藥物治療期間或之后疾病進(jìn)展的非小細(xì)胞肺癌患者。2024年,該產(chǎn)品相繼獲得FDA及中國(guó)CDE的突破性療法認(rèn)定,適用于既往接受過(guò)全身治療、具有活化HER2突變的晚期不可切除或轉(zhuǎn)移性NSCLC成人患者。
今年12月10日,勃林格殷格翰在2024年ESMO亞洲大會(huì)上公布了BEAMION LUNG-1試驗(yàn)1b期隊(duì)列1的最新研究數(shù)據(jù),評(píng)估zongertinib在治療攜帶人表皮生長(zhǎng)因子受體-2(HER2)突變陽(yáng)性晚期非小細(xì)胞肺癌經(jīng)治患者中的療效。
數(shù)據(jù)顯示,zongertinib(劑量為每日120毫克,單次服用,n=75例患者)展現(xiàn)出卓越療效:客觀緩解率(ORR)為71%,疾病控制率(DCR)達(dá)93%。初步生存數(shù)據(jù)表明,zongertinib緩解持久:6個(gè)月無(wú)進(jìn)展生存期(PFS)和緩解持續(xù)時(shí)間(DoR)分別為69%和73%。在數(shù)據(jù)截至?xí)r,仍有55%的患者仍在接受治療。隊(duì)列1的研究數(shù)據(jù)正持續(xù)完善中。
四川省醫(yī)藥保化品質(zhì)量管理協(xié)會(huì)組織召開
2025版《中國(guó)藥典》將于2025年10月..關(guān)于舉辦四川省藥品生產(chǎn)企業(yè)擬新任質(zhì)量
各相關(guān)企業(yè): 新修訂的《中華人..四川省醫(yī)藥保化品質(zhì)量管理協(xié)會(huì)召開第七
四川省醫(yī)藥保化品質(zhì)量管理協(xié)會(huì)第七..“兩新聯(lián)萬(wàn)家,黨建助振興”甘孜行活動(dòng)
為深入貫徹落實(shí)省委兩新工委、省市..學(xué)習(xí)傳達(dá)中央八項(xiàng)規(guī)定精神專題會(huì)議
2025年4月22日,協(xié)會(huì)黨支部組織召..關(guān)于收取2025年度會(huì)費(fèi)的通知
各會(huì)員單位: 在過(guò)去的一年里,..四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)急指
四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)..四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)急指
四川省應(yīng)對(duì)新型冠狀病毒肺炎疫情應(yīng)..