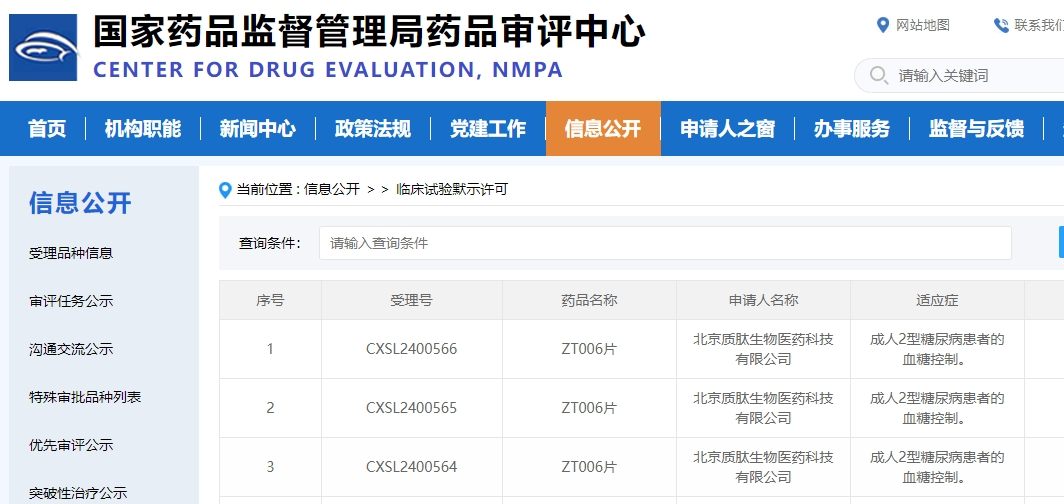
日前,根據國家藥監局藥審中心官網信息顯示,質肽生物1類新藥ZT006片獲得臨床試驗默示許可,擬開發用于成人2型糖尿病患者的血糖控制。
根據質肽生物官網介紹,ZT006是新一代口服蛋白藥品種,主要治療糖尿病和肥胖癥。經過優化的ZT006具有較高的生物利用度,有希望成為繼口服司美格魯肽之后的新一代口服GLP-1品種。口服給藥是公認的、可以顯著提高慢性病患者依從性的一種給藥方式。
據了解,質肽生物專注于開發治療慢性代謝性疾病(如糖尿病、肥胖、非酒精性脂肪性肝炎等)治療領域的創新生物藥,其產品管線基本圍繞GLP-1靶點展開。其中,質肽生物自主研發的GLP-1注射劑ZT002已在澳洲完成一期臨床研究,并于2023年分別獲批在國內開展糖尿病、減重以及治療阿爾茨海默病三項適應癥的臨床試驗。臨床實驗已經證明,該分子有望實現每月一次給藥。根據質肽生物方面的披露,ZT002是國內唯一進入臨床的每月給藥一次的GLP-1類藥物。
此外,質肽生物產品管線重還有一款司美格魯肽注射液生物類似藥ZT001,目前正在圍繞糖尿病和減重進行開發。2024年3月,愛美客全資子公司諾博特生物與質肽生物達成了技術授權及MAH合作協議,雙方決定共同推進ZT001減重適應癥在大中華地區的臨床申報和產業化生產。2023年11月,愛美客參與領投了質肽生物近2億元的B+輪融資.
今年5月,質肽生物又與通化東寶簽署合作協議,根據協議約定,后者將獲得前者ZT001用于治療2型糖尿病適應癥在中國大陸地區獨占權益,以及共同合作開發海外市場權利。合作產品在中國大陸地區上市后,通化東寶將成為合作產品在中國大陸地區的藥品上市許可持有人。目前,ZT001已在國內完成2型糖尿病適應癥的臨床I期,并啟動了與諾和泰在2型糖尿病患者中有效性和安全性的III期臨床研究。
質肽生物另一款GLP-1/FGF21雙靶點激動劑ZT003則是瞄準了治療手段幾乎空白的非酒精性脂肪性肝炎(NASH),該領域潛在藥物市場達到200億美元以上。不過,該藥物開發還處于早期階段,并未進入臨床試驗。
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..