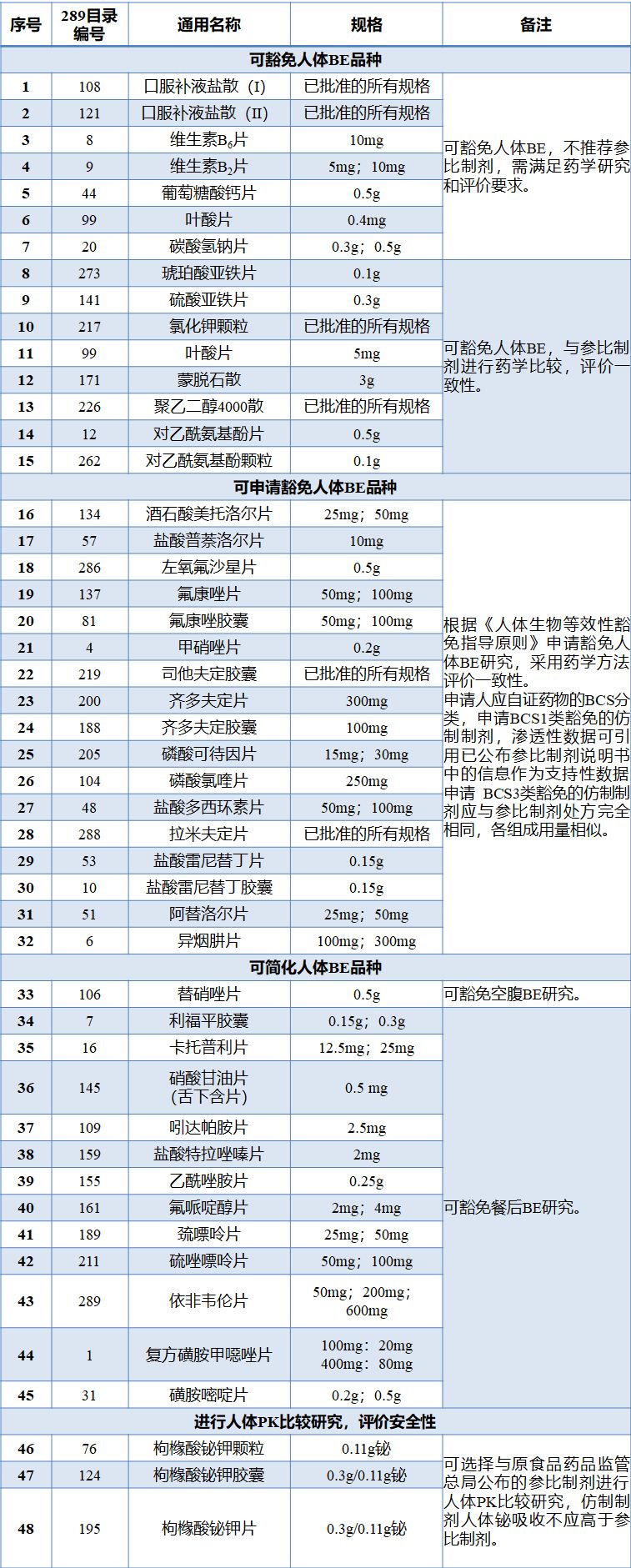
5月31日,為落實《關于仿制藥質量和療效一致性評價工作有關事項的公告》(國家食品藥品監督管總局公告2017年第100號)要求,國家藥品監督管理局正式發布《可豁免或簡化人體生物等效性(BE)試驗品種的通告(2018年第32號)》,確定了2018年底前需完成仿制藥一致性評價品種目錄中可豁免或簡化人體生物等效性(BE)試驗的48個品種大名單,其中,可豁免人體BE品種15個,可申請豁免人體BE品種17個,可簡化人體BE品種(包括可豁免空腹BE和可豁免餐后BE)13個,進行人體PK比較研究評價安全性品種3個。
可豁免或簡化人體生物等效性(BE)試驗品種
并非放寬標準
自2016年4月CFDA公開征求《人體生物等效性試驗豁免指導原則》的意見到同年5月正式稿發布起,醫藥行業一直翹首期盼《可豁免或簡化人體生物等效性試驗(BE)品種目錄》的發布。
按照《人體生物等效性試驗豁免指導原則》,藥品被分為四類,包括:“高溶解性、高滲透性”的BCS1類,“低溶解性、高滲透性”的BCS2類,“高溶解性、低滲透性” BCS3類和“低溶解性、低滲透性” BCS4類。其中1類和3類藥物,只要處方中其他輔料成分不顯著影響API吸收,則不必證明該藥物在體內生物利用度和生物等效的可能性。
業內專家對記者表示,BCS1類藥物需要證明藥物具有高溶解性和高滲透性,才能夠獲得生物等效性豁免,仿制藥和RLD必須均為快速溶出,且制劑中不含有影響主藥成分吸收速率和吸收程度的任何輔料;BCS3類的藥物則需要證明藥物具有高溶解性,仿制藥和RLD均能非常快速地溶出,且二者處方完全相同,組成成分用量相似,工藝放大、生產和上市后變更時,制劑處方也應當完全相同。
事實上,經過此前仿制藥質量和療效一致性評價辦公室經調研論證和征求意見,業內對于豁免BE或簡化BE絕非意味著放寬一致性評價標準已有共識。
“推薦豁免或簡化BE品種是基于BSC分類原則,體現了我國一致性評價的標準與國際標準接軌,對寬治療窗口的低風險產品合理豁免或簡化符合藥品本身的科學監管屬性。”某企業研發部門負責人對記者表示,公司已經有品種受理一致性評價申請,就是按照BSC分類原則申請簡化。
企業主動提速
去年11月11日,CDE曾發布《關于征求可豁免或簡化人體生物等效性試驗(BE)品種意見的通知》,共涉及57個產品,超過6000個批文,分為“豁免BE”和“簡化BE”兩類,其中可豁免BE品種44個;2017年12月18日,CDE再次發布通知,正式豁免了聚乙二醇4000相關產品的一致性評價臨床試驗。
為進一步提速仿制藥一致性評價工作,目前國家局已經發布幾十個一致性評價各類配套文件,并圍繞參比制劑進行了全面深入的梳理,陸續公布了多批參比制劑目錄,可以說自審評制改為備案制以來,產業和監管全鏈條的一致性評價推進速度均在明顯加快。
品種方面,此次正式發布的48個品種名單,批文數量比較集中的鹽酸雷尼替丁膠囊、甲硝唑片、對乙酰氨基酚片、異煙肼片、維生素B6片、維生素B2片等品種均列其中,聚乙二醇4000散、氯化鉀顆粒、琥珀酸亞鐵片、左氧氟沙星片等批文數量較少的品種也包括在內。
企業方面,據記者簡略查詢,此前確有不少一致性評價申請人按照豁免或簡化BE的路徑開展相關研究及申報,如:先聲藥業的蒙脫石散一致性評價申請已被受理;華潤雙鶴利民藥業(濟南)已經開展了替硝唑片的餐后BE研究;卡托普利片已有石藥集團歐意藥業申報一致性評價,常州制藥廠、山東新華制藥和山東羅欣藥業也已經啟動卡托普利空腹研究。
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..