4月28日,士澤生物宣布,其開發(fā)的異體通用“現(xiàn)貨型”iPSC衍生多巴胺能神經(jīng)前體細(xì)胞注射液(XS411注射液)的新藥注冊臨床試驗1期及2期申請,已獲中國國家藥品監(jiān)督管理局(NMPA)批準(zhǔn),用于治療早發(fā)性帕金森病。
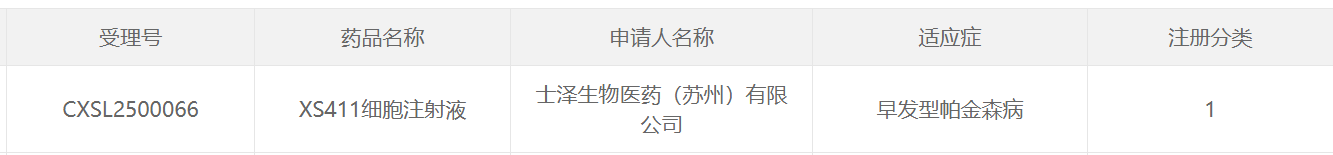
根據(jù)士澤生物新聞稿介紹,該公司將與醫(yī)院神經(jīng)科聯(lián)合開展“隨機(jī)雙盲對照”的iPSC再生多巴胺神經(jīng)前體細(xì)胞治療早發(fā)性帕金森病注冊臨床試驗。復(fù)旦大學(xué)附屬華山醫(yī)院王堅主任/陳亮主任/張菁主任作為牽頭PI及共同臨床負(fù)責(zé)人、蘇州大學(xué)附屬第二醫(yī)院劉春風(fēng)主任作為聯(lián)合中心及聯(lián)合負(fù)責(zé)PI合作開展。
公開數(shù)據(jù)顯示,帕金森病為全球第二大神經(jīng)退行性疾病,其中早發(fā)性帕金森病患者約占10%~15%,這部分患者起病年齡早且病程長,運(yùn)動并發(fā)癥早發(fā),患者家庭及社會負(fù)擔(dān)沉重,臨床存在急需滿足的臨床需求。
2024年,士澤生物與上海市東方醫(yī)院劉中民院長團(tuán)隊合作,已完成多例iPSC衍生細(xì)胞治療帕金森病患者(臨床隨訪期至今超過12個月)。士澤生物臨床級iPSC衍生多巴胺能神經(jīng)前體細(xì)胞經(jīng)帕金森病患者紋狀體殼核區(qū)移植治療中重度帕金森病最長隨訪期已超過12個月,長期臨床隨訪結(jié)果顯示無細(xì)胞療法相關(guān)不良事件出現(xiàn),且多例受試患者開關(guān)期時間及MDS-UPDRS評分量表等關(guān)鍵療效指標(biāo)及多項非運(yùn)動指標(biāo)均獲得顯著性改善。
四川省醫(yī)藥保化品質(zhì)量管理協(xié)會組織召開
2025版《中國藥典》將于2025年10月..關(guān)于舉辦四川省藥品生產(chǎn)企業(yè)擬新任質(zhì)量
各相關(guān)企業(yè): 新修訂的《中華人..四川省醫(yī)藥保化品質(zhì)量管理協(xié)會召開第七
四川省醫(yī)藥保化品質(zhì)量管理協(xié)會第七..“兩新聯(lián)萬家,黨建助振興”甘孜行活動
為深入貫徹落實(shí)省委兩新工委、省市..學(xué)習(xí)傳達(dá)中央八項規(guī)定精神專題會議
2025年4月22日,協(xié)會黨支部組織召..關(guān)于收取2025年度會費(fèi)的通知
各會員單位: 在過去的一年里,..四川省應(yīng)對新型冠狀病毒肺炎疫情應(yīng)急指
四川省應(yīng)對新型冠狀病毒肺炎疫情應(yīng)..四川省應(yīng)對新型冠狀病毒肺炎疫情應(yīng)急指
四川省應(yīng)對新型冠狀病毒肺炎疫情應(yīng)..