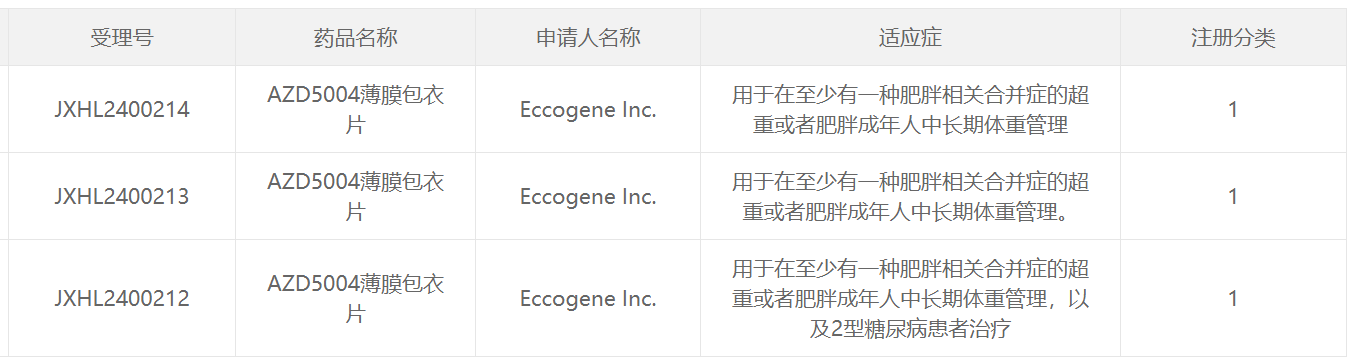
 圖片來源:CDE官網
圖片來源:CDE官網
AZD5004是一款每日一次、低劑量的小分子GLP-1受體激動劑,該藥物在臨床前研究中證明具有理想的療效和安全性。
2023年11月,阿斯利康與誠益生物達成獨家協議,以潛在超20億美元的總額獲得ECC5004(即AZD5004),用于治療包括肥胖癥、2型糖尿病和其他合并癥在內的適應癥。阿斯利康將獲得在中國以外的所有地區對ECC5004的任何適應癥的開發和商業化的獨家權利。在中國,誠益生物和阿斯利康將合作共同開發和商業化ECC5004。
此前的1期臨床試驗初步結果顯示,與安慰劑相較,AZD5004在低劑量10mg與30mg展現積極的減重與血糖降低效果,并具有>70%的口服生物利用度以及良好的耐受性。
近日(11月5日),阿斯利康公布了AZD5004在患有2型糖尿病的肥胖患者中進行的1期臨床試驗的最新結果。數據顯示,患者是否伴隨食物服用AZD5004均不會影響它的藥代動力學特征。探索性療效分析顯示,接受劑量為50mg的AZD5004治療的患者中,4周后患者體重與基線相比降低5.8%,約為9.4斤。同時,患者的空腹血糖等指標也有所下降。
阿斯利康彼時的新聞稿表示,這些數據支持AZD5004進入2期臨床試驗,在患有和不患有2型糖尿病的肥胖患者中進一步評估其減肥效果。同時,該公司還計劃將AZD5004與SGLT2抑制劑dapagliflozin聯用,治療2型糖尿病、慢性腎病和心力衰竭患者;AZD5004與口服PCSK9抑制劑AZD0780聯用具有進一步降低高風險心血管疾病的潛力。
本次這款小分子GLP-1受體激動劑在中國也獲批臨床,意味著其即將在中國開展注冊性臨床研究。
參考資料:
[1] 中國國家藥監局藥品審評中心官網. Retrieved Nov 12, 2024, from https://www.cde.org.cn/main/xxgk/listpage/da6efd086c099b7fc949121166f0130c
[2]誠益生物與阿斯利康達成獨家許可協議,進行心血管代謝疾病領域小分子GLP-1受體激動劑ECC5004的開發和商業化 . Retrieved Nov 9,2023,from https://mp.weixin.qq.com/s/r1geVAKanLOBNdJs8D1U8g
[3] AZN Meet the Management: Weight Management Virtual Event. Retrieved November 4, 2024, from https://www.astrazeneca.com/content/dam/az/Investor_Relations/events/Weight-Management-Virtual-Event-IR-presentation.pdf
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..