2024年的國家醫保談判正在進行中,這是國家醫保局成立以來牽頭的第7次國家醫保藥品目錄調整。
據國家醫保局此前公示,在今年7月1日至7月14日期間,共收到企業申報信息626份,涉及藥品(通用名,下同)574個,與2023年相比,申報藥品數量有所增加;經審核,440個藥品通過初步形式審查。
據罕見病信息網整理,在此前醫保局公布的初審名單罕見病藥物方面,至少有40個藥品通過初審。
如替度格魯肽(短腸綜合征)、醋酸氟氫可的松片(先天性腎上腺皮質增生癥和Addison病)、氯苯唑酸葡胺軟膠囊(轉甲狀腺素蛋白淀粉樣變性多發性神經病)、卡谷氨酸分散片&苯丁酸甘油酯(尿素循環障礙)、注射用培妥羅凝血素α(血友病)等。
其中,值得關注的是,12個罕見病有超過兩款以上的適應癥內藥物,包括進行性肌營養不良、肺動脈高壓、先天性腎上腺皮質增生癥(CAH)、神經母細胞瘤、嬰兒痙攣癥、地中海貧血、轉甲狀腺素蛋白淀粉樣變性多發性神經病(ATTR-PN)、視神經脊髓炎譜系疾病(NMOSD)、 陣發性睡眠性血紅蛋白尿癥(PNH)、原發免疫性血小板減少癥(ITP)和肝豆狀核變性。
需要說明的是,一個藥品通過初步形式審查,只代表其符合申報條件,具備了參與目錄調整的資格,不代表其已經進入了國家醫保藥品目錄。
形式審查是對申報藥品是否符合當年國家醫保藥品目錄調整申報條件以及藥品信息完整性進行的審核。根據工作安排,形式審查主要分為初審、初審結果公示、復審、復審結果公告四個步驟。
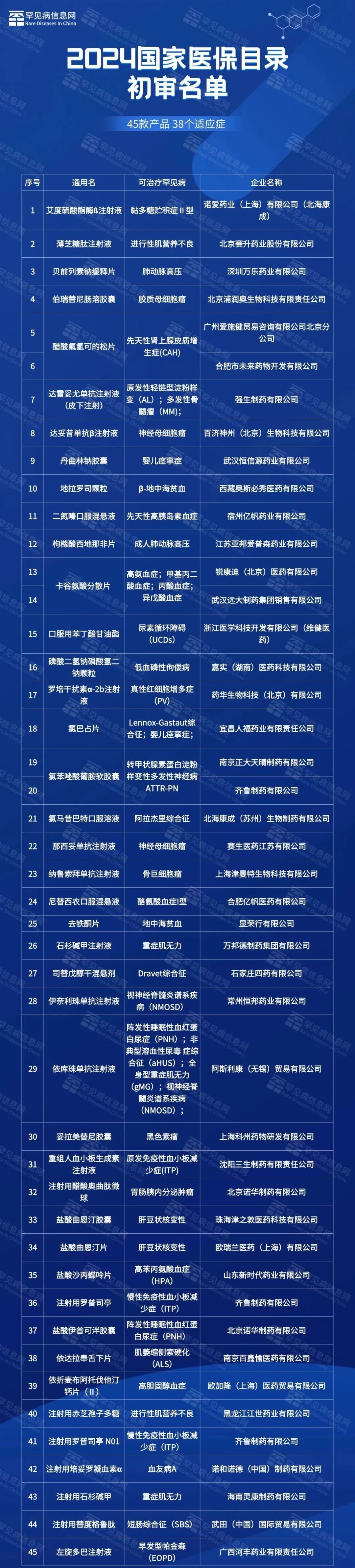
注:
1、數據來源于《2024年國家基本醫療保險、工傷保險和生育保險藥品目錄調整通過初步形式審查的申報藥品名單》;
2、5代表2024年6月30日前經國家藥監部門批準上市,說明書適應癥或功能主治中包含有衛生健康委《第一批罕見病目錄》《第二批罕見病目錄》所收錄罕見病的藥品。
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..