10 月 12 日,CDE 官網顯示,諾華的布西珠單抗 (Brolucizumab) 新適應癥在國內報上市,推測適應癥為濕性年齡相關性黃斑變性。
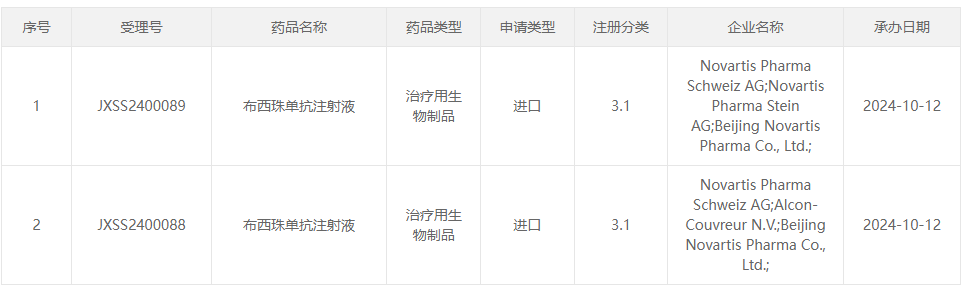
截圖來源:CDE 官網
布西珠單抗是由諾華研發的全 VEGF-A 抑制劑,是一種新型人源化單鏈抗體片段,分子量僅為 26kDa,親和力高、組織滲透力強、全身副反應小。2019 年 10 月 7 日在首次在美國獲批上市,用于治療濕性年齡相關性黃斑變性,2022 年 6 月,又獲批糖尿病黃斑水腫。
布西珠單抗在 FDA 的獲批基于 III 期 HAWK 和 HARRIER 臨床試驗的結果,在這些試驗中,布西珠單抗在第 1 年(第 48 周)的最佳矯正視力 (BCVA) 平均變化方面非劣于阿柏西普。
在兩項臨床試驗中,約 30% 的患者在第 1 年時視力增加了至少 15 個字母。在 HAWK 和 HARRIER 中,布西珠單抗早在第 16 周和第 1 年就顯示出中央亞區厚度 (CST) 的更大程度減少,并且更少的患者出現視網膜內 (IRF) 和/或視網膜下液體 (SRF)。視網膜液體是疾病活動的關鍵標志。
布西珠單抗的注射頻率為每 3 個月給藥 1 次,而雷珠單抗和阿柏西普都是每個月給藥 1 次,連續 3-5 次之后按需治療,所以布西珠單抗給藥頻次上有優勢。
目前,布西珠單抗尚未在中國獲批上市;2023 年 8 月已經在國內遞交了首個上市申請,推測適應癥為糖尿病黃斑水腫,預計 2025 年 Q1 獲批。
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..