作者:王興來 來源:蒲公英
前言:2017年底的時候總結了一篇關于清潔驗證的文章得到了很多人的認可,借著持續工藝確認流行的東風在2018年底制作了一張圖片闡述下我眼中驗證在質量管理中與其他板塊的關系,本圖繪制過程中感謝譚宏宇老師給出的修改意見及指導。
1、工藝驗證應當包括首次驗證、影響產品質量的重大變更后的驗證、必要的再驗證以及在產品生命周期中的持續工藝確認,以確保工藝始終處于驗證狀態,圖中用黑色虛線標準。
2、圖中的首次驗證和法規中的首次驗證不完全是同一概念,這里的首次驗證具體指的是變量不確定時開展的第一次驗證,包括新品種首次生產的驗證和工藝規程發生變更后的首次驗證,紅色實線代表著驗證過程一切按照預期順利進行的流程,當首次驗證成功后就可以開展持續工藝確認;
3、持續工藝確認的結果可以用來支持產品質量回顧分析,確認工藝驗證處于受控狀態。這就說明持續工藝確認實際上是產品質量回顧的部分數據分階段開展,個人認為持續工藝確認應當包括產品的關鍵質量屬性和關鍵工藝參數,如果需要個出處那就參考下注1,如圖中最右側用兩個綠色虛線和持續工藝確認建立聯系的魚骨圖部分,如下圖;
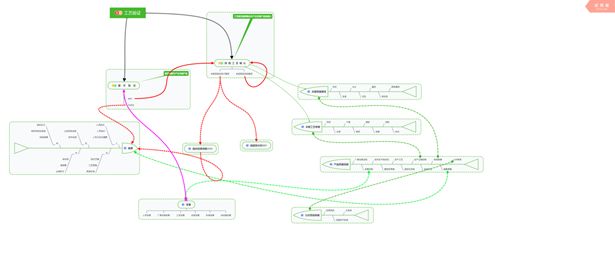
4、圖中右側同時也用綠色虛線將產品質量回顧與持續工藝確認關聯性做了標注,希望可以給大家帶來幫助,如下圖;
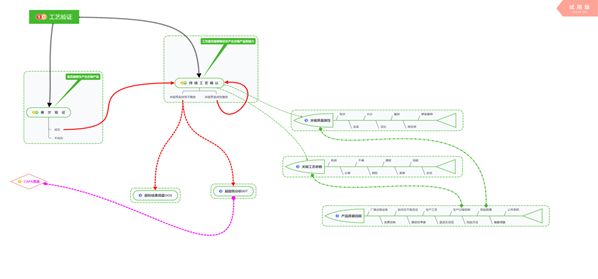
5、重點部分應該是圖中紅色虛線和粉色線體之間的較之關系,其中紅色虛線代表當驗證出現非預期情況時需要開展的工作與流程:
5.1當首次驗證不成功時那我們需要進行偏差調查,提出有效的CAPA并實施,然后因發生變更重新開展驗證,圖中用紅色虛線和粉色實線來標準本條的流程,如下圖;
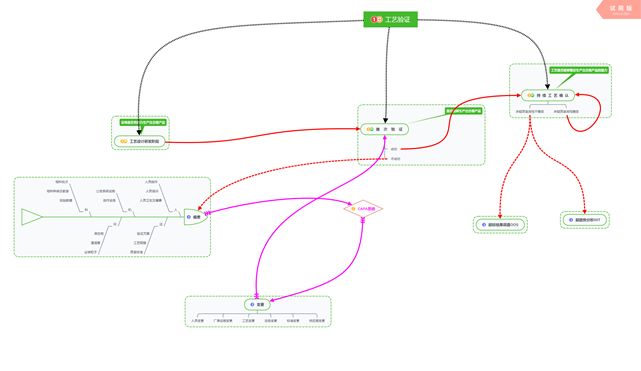
5.2當持續工藝確認出現問題時我們將其簡單的分為兩種情況即OOS和OOT;
5.2.1當出現OOS時我們需要啟動偏差調查,提出有效的CAPA并實施,然后因發生變更重新開展驗證,圖中用紅色虛線和粉色實線來標準本條的流程,如下圖;
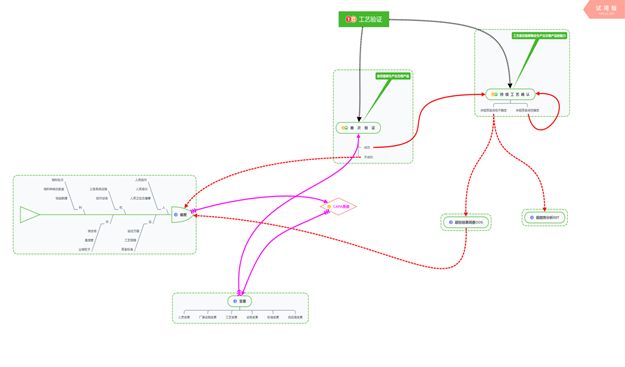
5.2.2當出現OOT時我們需要針對趨勢提出有效的CAPA(前提是這是個有意義的趨勢,當然這里邊還涉及持續工藝確認開展樣本數量不同和OOT情況出現的對比等情況),CAPA實施后因發生變更開展必要的再驗證,圖中用粉色虛線來標準本條的流程,如下圖;
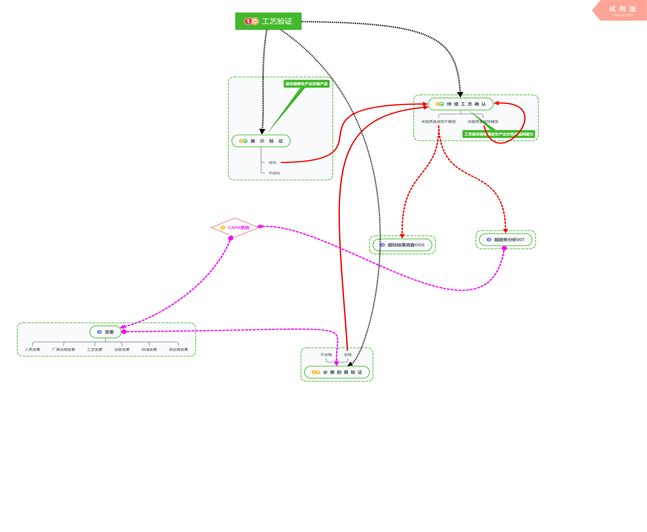
5.2.3需要解釋的是雖然OOT和OOS都執行CAPA 變更的流程,但是二者所變之情況還是有區別的,OOS是超出原范圍引起變更、OOT是在原范圍內的改進變更也可以說叫持續改進;
6、放行時我們需要審核的可以大致按照人、機、料、法、環、測等幾個方向來思考,這其中就包括了偏差、變更及相應的CAPA、關鍵質量屬性、關鍵工藝參數、公共系統等等,圖中用藍色虛線來鏈接相關項目的關系,如下圖;
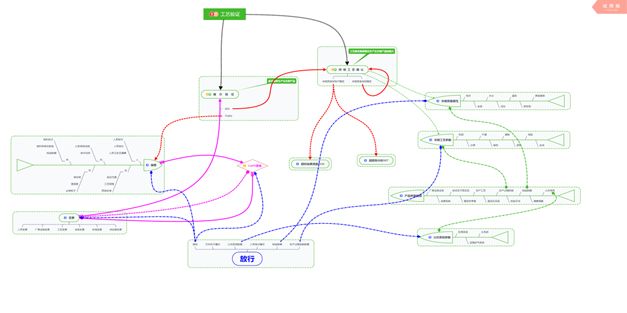
注:
1、引用PDA工藝驗證指南,An ongoing program to collect and analyze productand process data that relate to product quality must be established (§ 211.180(e)).必須建立一個持續和不斷發展的程序,收集和分析與產品質量有關的產品和工藝數據(§211.180(e))。
2、關鍵質量屬性:指某種物理、化學、生物學或微生物學的性質,應當有適當限度、范圍或分布,保證預期的產品質量
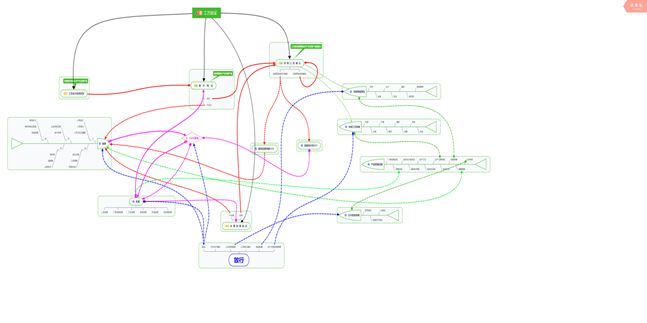
最后奉上這張本人繪制了半個多月的全圖,由于時間關系本次就暫不再圖中將取樣流程展開,如有不妥之處還望大家包涵,最后謝謝您的閱讀,也希望您多提出不足之處。
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..