3 月 13 日,CDE 官網顯示,禮來 1 類新藥 LY3549492 片的臨床申請獲得 CDE 受理。這是該藥首次在國內申報臨床。LY3549492 是一款胰高血糖素樣肽-1 受體(GLP-1R)非肽類激動劑(NPA),目前正在海外開展一項雙盲 Ⅱ 期臨床研究(NCT06683508),以比較每天使用一次 LY3549492 與安慰劑對肥胖或超重成人受試者進行體重管理的效果。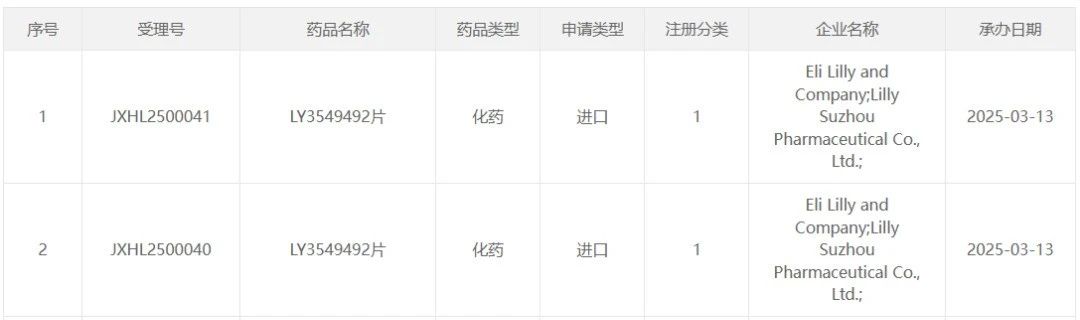
圖源:CDE 官網口服 GLP-1 是當前減肥藥領域竟爭的新高地。雖然諾和諾德的口服版司美格魯肽早已獲批上市,但其仍屬于多肽藥物,生物利用度仍有提升空間。此外,成本和產能也是傳統多肽藥物的弊端。與傳統的肽類 GLP-1R 激動劑相比,GLP-1R 非肽類小分子激動劑具有諸多優勢,包括:可口服給藥,提高患者依從性;生物利用度更高;化學穩定性高,在儲存和運輸中更穩定,不易降解;生產成本低,更容易實現大規模生產等等。因此,口服小分子 GLP1 已成為當下的研發熱點。禮來在該領域早有布局。除了 LY3549492,禮來開發的 Orforglipron(LY3502970)也是一種非肽類口服 GLP-1R 小分子激動劑,該藥可謂是小分子 GLP-1R 藥物的先驅。Orforglipron 最早由日本公司中外制藥株式會社研發,2018 年禮來以 5000 萬美元首付款拿到了它的全球開發和商業化權利。目前, Orforglipron 正在開展治療肥胖、2 型糖尿病,、阻塞型睡眠呼吸暫停等適應癥的 Ⅲ 期臨床,是研究進度最快的 GLP-1R 小分子激動劑。國內藥企中,恒瑞(HRS-7535)、聞泰醫藥/箕星藥業(VCT220)的 GLP-1R 小分子也已進入 Ⅲ 期。
