預先定義的藥品質量目標是什么?
配方與工藝的相互關系調整會對藥品關鍵屬性產生何種影響?
是否能回答上述問題?如果可以,那么你的答案來自哪里?來自研發工作研究得出的實驗數據、以及文獻上的知識嗎?是依據質量源于設計的原則嗎?
質量源于設計的一個關鍵元素就是“設計空間”的概念,其是能保證產品合理性能屬性的一個由產品設計和工藝變量構成多維空間。產品和工藝的變更只要不出這個空間,那么變更實施無需再批準。聽上去“設計空間”的概念很美麗,但現實卻很骨感,在實際研發、放大及規模商業化生產上,我們的科研人員和工程師遇到了很大的挑戰。
作者在文章中介紹如何將“設計空間”的概念在凍干工藝在研發、放大及轉移上進行應用。
1995 Chang 和Fischer 提出過一個確定凍干工藝設計空間的想法,如下圖
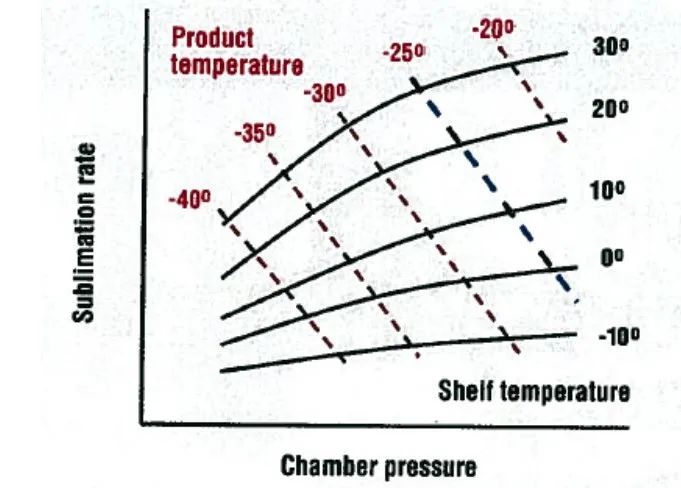
圖一
升華速率為X軸,Y軸體現箱體壓力,從而對產品溫度、板層入口溫度及箱體壓力之間的關系進行描述。要知道,箱體壓力對產品溫度和升華速率是有很復雜的影響:
1. 較高的箱體壓力將降低水汽從產品升華到箱體內的驅動力。這個驅動力可定義為產品冰界面內壓力與箱體壓力的壓力差(Pi-Pc)。從圖1中,可以看出,一定溫度的產品其升華速率隨箱體壓力的增加而線性降低。
2. 較高的箱體壓力將增加熱傳導率,也就是提高瓶底與板層之間細小縫隙中的氣體的熱傳導性。這種影響將會增加產品溫度,這會帶來產品冰內的氣體壓力的升高,從而提高冰界面內的水汽壓力。不難理解水汽升華至箱體內的驅動力也就提高了。
可見,較高箱體壓力最直接的作用是提高產品溫度和產品的升華速率,但需要意識到,這種作用所帶來的熱傳導能力的提高比升華速率的提高更具負面意義。因此,有效工藝是期望將初次干燥過程中的產品目標溫度能在最高的板層溫度和最低的箱體壓力間進行維持。
怎么測量升華速率
最傳統的方式是稱重測量。即凍干周期開始前,稱量一定量西林瓶的重量Wi,初次干燥完成后,再稱量Wp,然后用干燥時間t,計算平均升華速率(Wi-Wp)/ t。很顯然,這是一種破壞性試驗。
現在有一種過程分析技術應用于凍干工藝,即之前提到的TDLAS—— Tunable diode laser absorption spectroscopy 可調諧半導體激光吸收光譜技術,此裝置安裝于凍干箱體和冷阱之間的連接管(主閥區)上。基本原理是讓近紅外光束(near- infra red beam)與箱阱連接通路軸線成一定夾角,水的吸收波段多普勒頻移被測量,兩吸收峰值的頻移比例換算為水汽通過的速度。由于通徑已知,且水汽濃度也可以通過傳統吸收光譜法測出,從而得出瞬時水汽質量流量。
確定設計空間的邊界
1. 定義產品失敗模式
通常開發凍干周期是通過對一系列工藝條件(板層溫度、箱體壓力和時間)的組合進行產品生產試錯。常規設計上下限是圍繞板層溫度、箱體壓力和時間而制定的。但在質量源于設計的構想下,研發者必須對能生產出可接受產品的工藝條件圖有更深入的理解,通過對試驗批的極限條件進行挑戰,直到不合格產品產生來,來獲得這種理解。
最常見的產品失敗是由于凍干崩解。崩解多源于初次干燥時超出產品溫度上限(崩解溫度),已干燥的部分與粘稠流體混合,從而失去了預凍時形成的微觀結構。崩解是不可接受的現象,其會導致高水分殘留和很差結構屬性。對于大多數配方,初次干燥的產品溫度上限是共晶點溶解溫度。
2. 定義設計空間內的產品實施邊界
初次干燥時的產品溫度上限取決于配方屬性,我們可以通過低溫分析儀器和凍干顯微鏡來獲得。舉例,假設某配方產品,初次干燥時的產品溫度上限為-25度,我們將其在圖一中以虛線標出(見下面的圖2),定義為產品配方屬性所決定的設計空間實施邊界。
3. 定義設計空間內的設備實施邊界
通常情況,研發、中試和規模生產各自所用的設備使用者不是同一撥人,因此彼此并不了解和關心設備間的差異。比如,研發人員用實驗室型設備進行凍干周期開發,但他們并不考慮中試設備性能的限度;當凍干配方轉移到臨床樣品生產的公司后,會發現凍干周期并不能生產出合格產品,導致項目的延期。此現象很常見吧?這說明在周期開發時,我們就應將將來生產型設備的能力限度考慮進去。
設備能力的限度有很多種可能因素構成,比如箱阱通徑不一樣、冷阱制冷能力不同、冷阱冷凝面積不一樣, 循環系統加熱功率不同,板層熱損失或傳熱系數不同…
設備的性能限度不同會有不同的“最大”升華速率,因此其構成了設計空間內的一個水平上邊界。
這里還有一個更復雜的凍干機性能限度,這就是通過箱阱之間通路的汽流動力學。汽流的產生是由于箱阱間的壓差所引起的,通常越高的壓差帶來越快的水汽通過連接管路的流速。恒定水汽的質量流量通過管路,速度會加快,從而導致箱阱間的壓差持續降低。但熱力學顯示,這個速度的限度與水汽氣中的聲速(400m/s, 1馬赫)相對應,當水汽速度接近1馬赫,水汽流量將會被阻塞,下游壓力再下降也不會影響通過管路的質量流量。凍干過程中,一旦流量被阻,將會導致凍干箱體內的壓力失控。
與其它設備性能限度不同,由于氣流阻塞所帶來的能力限度與系統壓力有關,質量流量的阻塞點(chokepoint)與壓力成直接比例關系,此邊界在設計空間上的大概形態以實線在圖中標出。
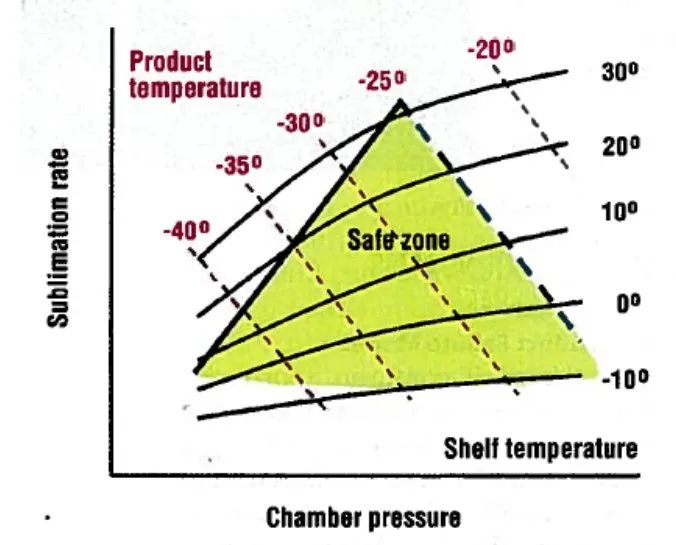
圖二
因此,以這個產品為例,設計空間由右側的產品邊界和左側氣流阻礙邊界(設備)構成,任何空間內的工藝條件都應可接受,當然,空間頂點區域附近是最有效的工藝條件。
進行一系列凍干機捕冰能力測試是很好的驗證設備能力限度的方式。在設定的壓力下,對板層線性斜率升溫,在某時刻,箱體控制壓力失控,這就是與阻塞點有關。為了評估此設備在此設定壓力下所能支持的升華速率,需要不斷測試,找到正確的壓力與板層溫度的關系,直到初始冰量的很大一部分已經被升華。然后再設定一個新的壓力控制點進行測試,直到收集足夠的數據能繪出圖中的阻礙點線。
當然,TDLAS可以有效減少此設備能力驗證的工作量,理論講其可以在一次捕冰實驗中確定出阻礙點曲線。
此外,檢測設備在捕冰測試中其它能力也是有必要的,比如檢測冷阱溫度是否維持在特定溫度下,如-50. 這些設備能力限度會體顯為設計空間的水平線。
最后,要生成一個像文中提及的設計空間,需要對配方和設備有深入的理解,這也是QbD質量原因設計所追求的。
此文翻譯摘抄自 Steven L. Nail, Jim A. Searles, 2008年 在 International BioPharm 上發表的 Elements of Quality by Design in Development and Scale-up of Freeze- Dried Parenterals
1
本文來源于拾西,由“制藥業”平臺整理發布,僅供交流學習,轉載請注明出處。歡迎關注“制藥業”公眾號,獲得最新制藥業創新技術、新聞動態等熱點話題。
四川省醫藥保化品質量管理協會組織召開
2025版《中國藥典》將于2025年10月..關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..