各相關單位:
藥品質量受權人制度是藥品生產企業授權其藥品質量管理人員對藥品質量管理活動進行監督和管理,對藥品生產的規則符合性和質量安全保證性進行內部審核,并由其承擔藥品放行責任的一項制度。實行藥品質量受權人制度是強化藥品生產企業內部質量管理機制,明確質量責任,提高企業質量管理水平的有效措施,也是進一步強化企業是質量第一責任人責任意識的有效手段。
按照省局質量受權人制度實施工作部署以及協會2012年培訓計劃,擬在2012年4月上旬及2012年下半年,舉辦兩次藥品質量受權人培訓班,第一期主要是對藥品質量受權人進行職能職責、工作范圍與內容等方面的基礎培訓;第二期主要是進行現代藥品質量管理方法的培訓。
現將有關事宜通知如下:
一、培訓對象:藥品生產企業(除中藥飲片生產企業外)質量受權人;藥品生產企業符合質量受權人任職條件,但尚未參加質量受權人資格培訓的人員。
企業質量受權人有特殊原因不能參加培訓的,應向省局安監處請假;企業因故未能設置藥品質量受權人的,應向省局安監處作出書面說明。
二、培訓內容:
第一部分基礎培訓
(一)國內外藥品質量受權人制度介紹;
(二)藥品質量受權人道德規范責任;
(三)產品放行權的行使;
(四)質量管理體系的建立與溝通;
(五)藥品投訴、召回與不良反應識別
(六)藥品生產驗證與產品質量趨勢分析
(七)企業內部自檢與外部質量審計
第二部分藥品質量的現代管理方法培訓
(八)長期趨勢分析與風險管理的數理基礎知識
(九)年度質量回顧與偏差分析;
(十)高風險藥品質量控制與案例分析;
(十一)藥品驗證管理與案例分析;
(十二)偏差處理與案例分析;
(十三)醫療機構臨床用藥管理
(十四)藥品供應鏈質量控制體系
師資由優秀藥品質量受權人、GMP專家、合資企業生產質量管理專家擔任。
三、培訓形式:課堂授課。培訓結束后,由四川省醫藥保化品質量管理協會頒發藥品《質量授權人培訓合格證書》。
四、培訓時間:預計培訓時間在第一期:2012年4月上旬;第二期:9月中旬,每期培訓三天。
五、報名方式及第一期報名截止時間(第二期另行通知)
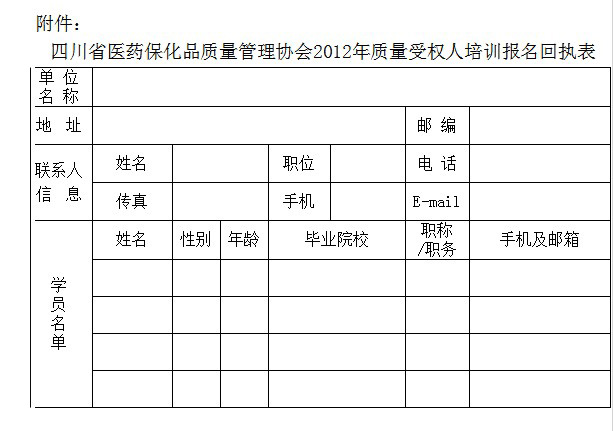
1、填好回執請于2012年3月2日前以傳真或網上郵箱方式將回執發至四川省醫藥保化品質量管理協會。
2、協會收到報名回執后,按報名人員通知培訓的具體時間、地點、費用。
六、聯系方式
聯 系 人:雷老師陳老師
電話:028-86919092
傳真:028-86919092
郵箱:scyyzx@163.com
特此通知!
四川省醫藥保化品質量管理協會
二0一二年一月四日